Introduction
La rééducation par assistance robotisée est récente (fin des années 90). Elle offre une assistance électromécanique au patient et consiste en la réalisation de mouvements passifs ou volontaires avec une aide ou une résistance. On note que ce genre d’outil est parfois associé à système de feedback pour le membre supérieur (plus occasionnellement pour le membre inférieur) afin d’offrir un retour au patient de son action.
L’assistance robotisée guide un mouvement qui est soumis à des degrés de liberté variables. La récupération de la marche est astreinte à un contrôle important tandis que les mouvements de préhension du membre supérieur sont plus libres. L’emploi de ce genre de thérapie permet une répétition importante d’actions avec un but final concret (saisie d’un objet, marche…).
L’utilisation de ce type de réentraînement offre la possibilité de travailler avec un public fragile et faible. La demande attentionnelle et physique est réduite du fait de la possibilité d’accompagner le mouvement et de mettre en décharge partielle les membres faibles.
Le travail en décharge
Les prémices de la robotique dans les domaines de la rééducation ont été initiées par les travaux sur l’entraînement en décharge ou en « suspension ». Placer le corps ou le membre d’un sujet en suspension partielle ou totale lui permet d’effectuer des gestes dirigés sans la contrainte de la pesanteur. Le patient se concentre spécifiquement sur le recouvrement d’un mouvement et l’exécution de son programme moteur.
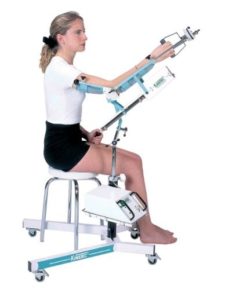
Les études concernant la rééducation fonctionnelle du membre supérieur en suspension ont été favorisées par le développement de systèmes articulés. Ils permettent au patient de ne pas « porter » leur bras et d’effectuer des tâches fonctionnelles avec des degrés de liberté importants. Il est démontré, sur le membre parétique du patient AVC chronique, que l’utilisation de ce type d’appareil permet de diminuer significativement le temps mis pour saisir un objet (Seo et al., 2009). Les auteurs proposent ce genre de protocole pour limiter la fatigue du patient et augmenter le nombre de répétitions sur des tâches orientées. D’autres études ont montré l’intérêt de ce travail auprès de patients souffrant d’une parésie importante du membre supérieur pour le maintien des amplitudes articulaires, la conservation de la fonction de saisie, l’augmentation de la vitesse de déplacement, et ceci, sans effets néfastes sur la force musculaire de l’épaule (Beer et al., 2007; Housman et al., 2009; Prange et al., 2011). L’utilisation de cette méthode sur des patients en phase subaigüe ne semble cependant pas apporter d’amélioration sur la distance maximale de saisie d’un objet, les capacités fonctionnelles globales du membre supérieur, ainsi que sur les paramètres algiques par rapport à des soins traditionnels.
Le principe de décharge partielle a été exploré de façon importante dans le cadre de la récupération de la marche. Globalement, les effets observés sont contrastés entre le travail à poids de corps et le travail en décharge. Certaines études ne ressortent aucun effet entre une prise en charge traditionnelle et l’utilisation du travail en décharge (Mehrholz et al., 2014; Nilsson et al., 2001). Cependant, ces résultats ont un intérêt dans le sens où la suppression d’une partie du poids de corps peut rendre plus accessible la rééducation à des personnes fragiles, dans un cadre sécuritaire et sans perte d’efficacité du traitement.
Parallèlement, d’autres auteurs tendent à montrer des effets positifs de la rééducation en décharge partielle par rapport à une rééducation classique (Liu et al., 2014; McCain et al., 2008; Takao et al., 2015). Il y est reporté une modification de l’angle de pennation des muscles tibialis antérieur et gastrocnémien (partie médiale) permettant un développement de force supérieur, ainsi qu’un gain de vélocité et d’endurance sur les tests de marche. Cependant, aucun changement des paramètres spatio-temporaux de marche n’est démontré (cadence et longueur de pas).
La grande variabilité des protocoles sur le niveau de décharge, l’ancienneté de l’AVC du patient, ses capacités de déambulation, etc. sont autant de paramètres pouvant influer sur les résultats de la prise en charge. Il est généralement conseillé d’utiliser des niveaux de décharge compris entre 15 et 30% du poids de corps (40% maximum) et de programmer une vitesse de marche sur tapis proche des capacités fonctionnelles du patient en situation de marche normale. (Hesse, 2008; Sullivan et al., 2002). Par ailleurs, il semblerait que les patients AVC ayant récupéré une fonction de marche tirent davantage profit de ce principe de rééducation que ceux ne l’ayant pas ou peu retrouvée.
L’assistance robotisée et exosquelette
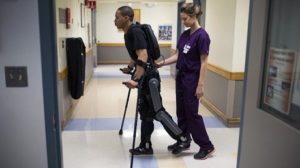
L’objectif est de stimuler des fonctions déficientes et de rééduquer l’ensemble des processus neuro-moteurs. L’exosquelette peut-être considéré comme une orthèse, dans le sens où le dispositif ne remplace pas les membres ou les articulations mais, au contraire, les soutient et les assiste. L’efficacité de l’assistance robotisée pour la marche est soumise à de fortes discussions.Que ce soit au niveau du bras ou de la marche, l’évolution des dispositifs de décharges a été l’assistance robotisée puis les exosquelettes. L’intérêt de ce type d’appareils est de pouvoir programmer, au choix et suivant les dispositifs, une mobilisation passive des membres lésés, d’assister le mouvement, ou d’offrir une résistance à la production d’un mouvement.
Une des premières publications portant sur ce type de rééducation montre un effet favorable (contre placebo) sur la récupération motrice et la mobilité proximale du membre supérieur chez des patients AVC au stade aigu. Cette étude suggère donc de poursuivre les évaluations afin de justifier l’utilisation d’une assistance robotisée auprès de patients hémiparétiques (Aisen et al., 1997).
Ces résultats ont été confirmés par d’autres auteurs (Mehrholz et al., 2012; Volpe et al., 2000). Cependant, plusieurs études et revues de littérature sur le sujet vont dans le sens inverse et affirment que l’assistance robotisée et l’utilisation d’exosquelettes ne présentent pas plus d’effets positifs sur la récupération des capacités fonctionnelles du bras parétique qu’une prise en charge classique et des soins habituels prodigués en kinésithérapie (Kwakkel et al., 2008; Lo et al., 2010; Masiero et al., 2011).
Dans la même idée, plusieurs études semblent être en accord sur le fait que l’assistance robotisée ne permet d’obtenir ni une augmentation significative systématique sur la fonction des membres inférieurs, ni une amélioration de l’autonomie supérieure à un traitement en kinésithérapie traditionnelle (Hidler et al., 2009; Mehrholz et al., 2008; Swinnen et al., 2014).
Connecté au système neuromoteur, l’exosquelette peut être en mesure de commander et d’assister la production de mouvements en recueillant, en analysant et en traduisant les signaux EMG du patient (Cavallaro et al., 2006). Le système robotisé est donc sous le contrôle volontaire du patient. Il fonctionne comme un complexe musculaire en parallèle des muscles du patient afin de fournir une force additionnelle. Ce type de dispositif est un outil de rééducation et de réduction de la situation de handicap très prometteur, à la fois pour les patients AVC mais aussi pour d’autres pathologies (paraplégies, amputations…).
Pour une rééducation de la préhension, les études proposent de placer les électrodes soit sur les fléchisseurs et les extenseurs du poignet parétique (Song et al., 2013) dans le cas d’un contrôle en direct, soit sur le poignet sain dans le cas d’un contrôle par le membre controlatéral (Leonardis et al., 2015). Dans les deux situations les auteurs montrent une amélioration des capacités du mouvement de la main et de saisie d’objet avec une amélioration de la force de préhension. Ce modèle, très récent, présente des résultats encourageants pour la prise en charge des patients AVC sur les fonctionnalités du membre supérieur.
Conclusion
Le progrès des sciences dans les systèmes automatisés et dans la robotique a permis d’employer des moyens techniques de plus en plus aboutis dans le domaine de la rééducation. Cependant, ce type de robot a un coût encore relativement important (hautes technologies vendues en petit nombre). De plus, leur encombrement et leur manque de mobilité les cantonnent souvent aux soins dans les grandes unités de rééducation.
Comme nous l’avons constaté, les effets thérapeutiques sont discutés. Le ratio prix d’investissement/bénéfices patient reste encore à démontrer par rapport à d’autres outils disponibles. Il est néanmoins important de noter que ces appareils permettent de travailler de façon précoce et dans un environnement sécuritaire pour le patient.
Pour l’AVC, les robots de rééducation ont pour objectif d’aider et de prolonger l’action du thérapeute. L’intérêt est principalement du à la suspension du poids ou à l’aide motrice qu’ils fournissent. Ces outils privilégient la prise en charge des patients présentant des déficits sévères et une récupération motrice faible ou modérée.
Au regard de leurs résultats et de leur large champ d’application, les exosquelettes contrôlés myo-électriquement semblent néanmoins offrir des perspectives prometteuses. Il sera intéressant de suivre leurs évolutions. Cependant, le prix de ce type de dispositif ne permet pas, pour l’heure, d’imaginer une démocratisation de son utilisation dans le cadre de la rééducation.
Bibliographie
Aisen, M.L., Krebs, H.I., Hogan, N., McDowell, F., Volpe, B.T., 1997. The effect of robot-assisted therapy and rehabilitative training on motor recovery following stroke. Arch. Neurol. 54, 443–446.
Beer, R.F., Ellis, M.D., Holubar, B.G., Dewald, J.P.A., 2007. Impact of gravity loading on post-stroke reaching and its relationship to weakness. Muscle Nerve 36, 242–250.
Cavallaro, E.E., Rosen, J., Perry, J.C., Burns, S., 2006. Real-time myoprocessors for a neural controlled powered exoskeleton arm. IEEE Trans. Biomed. Eng. 53, 2387–2396.
Hesse, S., 2008. Treadmill training with partial body weight support after stroke: a review. NeuroRehabilitation 23, 55–65.
Hidler, J., Nichols, D., Pelliccio, M., Brady, K., Campbell, D.D., Kahn, J.H., Hornby, T.G., 2009. Multicenter randomized clinical trial evaluating the effectiveness of the Lokomat in subacute stroke. Neurorehabil. Neural Repair 23, 5–13.
Housman, S.J., Scott, K.M., Reinkensmeyer, D.J., 2009. A randomized controlled trial of gravity-supported, computer-enhanced arm exercise for individuals with severe hemiparesis. Neurorehabil. Neural Repair 23, 505–514.
Kwakkel, G., Kollen, B.J., Krebs, H.I., 2008. Effects of robot-assisted therapy on upper limb recovery after stroke: a systematic review. Neurorehabil. Neural Repair 22, 111–121.
Leonardis, D., Barsotti, M., Loconsole, C., Solazzi, M., Troncossi, M., Mazzotti, C., Parenti Castelli, V., Procopio, C., Lamola, G., Chisari, C., Bergamasco, M., Frisoli, A., 2015. An EMG-controlled robotic hand exoskeleton for bilateral rehabilitation. IEEE Trans. Haptics.
Liu, P., Wang, Y., Hu, H., Mao, Y., Huang, D., Li, L., 2014. Change of muscle architecture following body weight support treadmill training for persons after subacute stroke: evidence from ultrasonography. BioMed Res. Int. 2014, 270676.
Lo, A.C., Guarino, P.D., Richards, L.G., Haselkorn, J.K., Wittenberg, G.F., Federman, D.G., Ringer, R.J., Wagner, T.H., Krebs, H.I., Volpe, B.T., Bever, C.T., Bravata, D.M., Duncan, P.W., Corn, B.H., Maffucci, A.D., Nadeau, S.E., Conroy, S.S., Powell, J.M., Huang, G.D., Peduzzi, P., 2010. Robot-assisted therapy for long-term upper-limb impairment after stroke. N. Engl. J. Med. 362, 1772–1783.
Masiero, S., Armani, M., Rosati, G., 2011. Upper-limb robot-assisted therapy in rehabilitation of acute stroke patients: focused review and results of new randomized controlled trial. J. Rehabil. Res. Dev. 48, 355–366.
McCain, K.J., Pollo, F.E., Baum, B.S., Coleman, S.C., Baker, S., Smith, P.S., 2008. Locomotor treadmill training with partial body-weight support before overground gait in adults with acute stroke: a pilot study. Arch. Phys. Med. Rehabil. 89, 684–691.
Mehrholz, J., Hädrich, A., Platz, T., Kugler, J., Pohl, M., 2012. Electromechanical and robot-assisted arm training for improving generic activities of daily living, arm function, and arm muscle strength after stroke. Cochrane Database Syst. Rev. 6, CD006876.
Mehrholz, J., Platz, T., Kugler, J., Pohl, M., 2008. Electromechanical and robot-assisted arm training for improving arm function and activities of daily living after stroke. Cochrane Database Syst. Rev. CD006876.
Mehrholz, J., Pohl, M., Elsner, B., 2014. Treadmill training and body weight support for walking after stroke. Cochrane Database Syst. Rev. 1, CD002840.
Nilsson, L., Carlsson, J., Danielsson, A., Fugl-Meyer, A., Hellström, K., Kristensen, L., Sjölund, B., Sunnerhagen, K.S., Grimby, G., 2001. Walking training of patients with hemiparesis at an early stage after stroke: a comparison of walking training on a treadmill with body weight support and walking training on the ground. Clin. Rehabil. 15, 515–527.
Prange, G.B., Krabben, T., Stienen, A.H.A., van der Kooij, H., Rietman, J.S., Buurke, J.H., 2011. An explorative study into changes in circle drawing after gravity compensation training in chronic stroke patients. IEEE Int. Conf. Rehabil. Robot. Proc. 2011, 5975402.
Seo, N.J., Rymer, W.Z., Kamper, D.G., 2009. Delays in grip initiation and termination in persons with stroke: effects of arm support and active muscle stretch exercise. J. Neurophysiol. 101, 3108–3115.
Song, R., Tong, K., Hu, X., Zhou, W., 2013. Myoelectrically controlled wrist robot for stroke rehabilitation. J. Neuroengineering Rehabil. 10, 52.
Sullivan, K.J., Knowlton, B.J., Dobkin, B.H., 2002. Step training with body weight support: effect of treadmill speed and practice paradigms on poststroke locomotor recovery. Arch. Phys. Med. Rehabil. 83, 683–691.
Swinnen, E., Beckwée, D., Meeusen, R., Baeyens, J.-P., Kerckhofs, E., 2014. Does robot-assisted gait rehabilitation improve balance in stroke patients? A systematic review. Top. Stroke Rehabil. 21, 87–100.
Takao, T., Tanaka, N., Iizuka, N., Saitou, H., Tamaoka, A., Yanagi, H., 2015. Improvement of gait ability with a short-term intensive gait rehabilitation program using body weight support treadmill training in community dwelling chronic poststroke survivors. J. Phys. Ther. Sci. 27, 159–163.
Volpe, B.T., Krebs, H.I., Hogan, N., Edelstein OTR, L., Diels, C., Aisen, M., 2000. A novel approach to stroke rehabilitation: robot-aided sensorimotor stimulation. Neurology 54, 1938–1944.







Bonjour , je suis responsable d’un cabinet de kinésithérapie au Gabon en Afrique centrale j’apj’apprécie tous ces appareils. Comment faire pour les avoir ? Merci.